挨拶
第24回の抗悪性腫瘍薬開発フォーラムを、2018年3月31日(土)に開催いたします。
今回のフォーラムは、高橋俊二実行委員長(がん研有明病院)、北川洋副実行委員長(EFPIA-J/ノバルティスファーマ株式会社)、日野敬晴副実行委員長(EFPIA-J/アストラゼネカ株式会社)を迎え、「新制度の動向と抗がん剤開発へのインパクト~臨床研究法の施行等を見据えた対応と抗がん剤開発への影響分析~」をテーマに、準備を進めております。
是非ご参加いただけますようお願いいたします。
抗悪性腫瘍薬開発フォーラム
代表 武藤徹一郎
公益財団法人がん研究会
第24回抗悪性腫瘍薬開発フォーラムについて
2017年4月に新たな制度として、臨床研究の実施手続きや資金提供に関する情報公表のための「臨床研究法」が制定・公布されました。この法律により、特定臨床研究と呼ばれる新たな臨床研究のカテゴリーが設置され、臨床研究における安全性措置、資金提供に関連して製薬企業等が講ずべき措置についても定められることとなりました。しかしながら、臨床研究実施施設や関連する製薬企業に対して、ひいては新薬開発へ具体的にどういった影響があるのかは明らかではありません。
加えて、昨今の技術進歩に伴い新たな制度への議論として、疾患レジストリが取り上げられることが目に付くようになってきました。本フォーラムでは『新制度の動向と抗がん剤開発へのインパクト~臨床研究法の施行等を見据えた対応と抗がん剤開発への影響分析~』と題し、フォーラム開催時点での臨床研究法の内容を確認しながら、がん領域における法施行により想定される課題・解決方法について議論するとともに、臨床研究や疾患レジストリを抗がん剤開発へどのように活用すべきかについても議論を行いたいと思います。
第24回抗悪性腫瘍薬開発フォーラム
実行委員長 高橋俊二
がん研有明病院
開催概要
| 名称 | 第24回抗悪性腫瘍薬開発フォーラム 『新制度の動向と抗がん剤開発へのインパクト~臨床研究法の施行等を見据えた対応と抗がん剤開発への影響分析~』 |
|---|---|
| 日時 | 2018年3月31日(土) 午後1時~ |
| 会場 | 吉田富三記念講堂及びセミナー室AB (公益財団法人がん研究会がん研究所1F)アクセス 〒135-8550 東京都江東区有明3-8-31 最寄り駅:有明(ゆりかもめ)、国際展示場(りんかい線) |
| 参加費 | 4,000円(ミキサー費含む) 本フォーラムへの参加は事前登録制となっております。 |
| 参加受付 | 参加受付締切:2018年3月2日(金) ※定員になり次第、締め切らせていただきます。 |
| 参加申込み 方法 |
1. HPより参加登録をする。 2. 事務局より締切後、一週間程度で参加確認書をメールにて送信 3. 当日参加確認書を持参の上、参加費を受付で納入 ※上記の方法がとれない方は事務局にご相談下さい。 |
| 事務局 | 〒135-8550 東京都江東区有明3-8-31 (公財)がん研究会がん化学療法センター 担当:三原 TEL:03-3570-0661 FAX:03-3570-0484 E-mail: atdd-frm@jfcr.or.jp |
第24回抗悪性腫瘍薬開発フォーラム参加登録フォーム
参加登録は締め切りました。
プログラム
第24回フォーラムアンケートまとめ
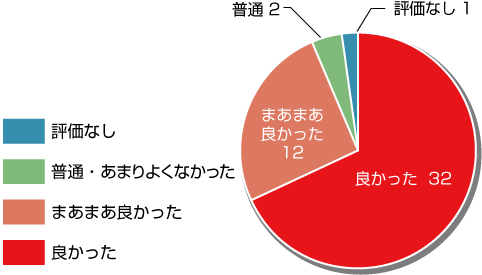
感想・意見
総合評価「良かった&まあまあ良かった」と回答
- 臨床研究法について詳しい内容と今後の課題がよくわかった(他19件)
- レジストリーについては不透明な問題(質やグローバル化etc)はあるが、問題点の整理につなげることができた(他5件)
- タイムリーな話題で興味深い内容だった(他5件)
- 産官学の総合的な視点から学べたのが良かった(他3件)
- もう少し演題数を少なくした方が良かった(他1件)
- 総合討論が良かった(他1件)
- ドラッグラグが発生しないよう、柔軟な対応を求めます
- Entrectinibはchampion caseと思うが今後このスキームをリードできる(話が日本に始めに来る)状況を作ることが必要と感じ。
- 臨床研究法については、少し情報として足りなかったので、“まあまあ”とします。ただ、開発として使えるとは考えなかったので、そこは新しい視点であった
- 法の規制で、臨床研究のハードルを上げたのはある意味必要だったのかと思うが、そのdataを何に使えるのか、何を目指しているのかがよくわからない
総合評価「普通」と回答
- 臨床研究法に関して厚労省の回答が不明確であったため
- 「未承認」をGCPか特定臨床研究か、どちらで実施すべきか?想定されている事例も不明?
今後取り上げるべき、興味のあるテーマ
【ゲノム医療】
- ゲノム医療の未来、データベースの利活用
- ファーマジェネティックの今後の考え方
- データベース研究について
- プレシジョンメディシンでがん組織の変異型と全身の免疫状態との組み合わせということは成り立つのか?治療薬の組み合わせレジメに対する判断法はあるのか
- ゲノム時代の疾患分類と規制(薬事承認)→疾患分類の概念が変わり、どの適応で承認を取るのか難しくなっている
- NGSの保険償還の話
【診断・治療法など】
- がん免疫環境のコントロールとcureを目指して
- Io剤の臨床評価方法
- 新規モダリティによる治療の進歩
- 早期癌の治療法(薬)の早期開発に向けて(エンドポイント等)
- 疾患レジストリに合った治療(薬剤)の有効度、ファーストライン、セカンドラインとの見直し
- 診断の進歩
【規制、承認、制度など】
- 日本におけるTissue agnosticな承認申請の現状と展望
- 今日ありました効能効果の追加について、申請を必要とするのかどうかの議論
- 日本のPatient アクセス制度の改善。拡大治験、患者申し出だけでは到底十分ではないため
- 「医療情報」の取り扱いについて、要配慮個人情報がビッグデータ法で示す個人を特定するデータとならないのか?
- 患者症例データを海外データと併合解析する上での課題
第24回フォーラム実行委員会
| 委員長 | 高橋 俊二(がん研有明病院) |
|---|---|
| 副委員長 | 北川 洋(EFPIA-J/ノバルティスファーマ株式会社) 日野 敬晴(EFPIA-J/アストラゼネカ株式会社) |
| 委員 | 井口 豊崇(医薬品医療機器総合機構) 稲垣 治(製薬協/アステラス製薬株式会社) 川村 学(PhRMA/日本イーライリリー株式会社) 慶徳 理枝子(EFPIA-J/ヤンセンファーマ株式会社) 河野 典厚(日本医療研究開発機構) 高見 朋子(PhRMA/MSD株式会社) 田村 研治(国立がん研究センター中央病院) 土井 俊彦(国立がん研究センター東病院) 中西 洋一(九州大学) 西尾 和人(近畿大学) 橋本 順一(製薬協/大塚製薬株式会社) 吉野 孝之(国立がん研究センター東病院) 渡辺 勝(PhRMA/MSD株式会社) 清宮 啓之(がん研究会) 冨田 章弘(がん研究会) 藤田 直也(がん研究会) |