挨拶
第19回の抗悪性腫瘍薬開発フォーラムを、2015年6月20日(土)に開催いたします。
山田雅信実行委員長(医薬品医療機器総合機構)、土井俊彦副実行委員長(国立がん研究センター東病院)、大熊伸一副実行委員長(米国研究製薬工業協会/日本イーライリリー株式会社))を迎え、「臨床研究を取り巻く新局面と臨床試験に対する支援のあり方」をテーマに準備を進めております。
是非ご参加いただけますようお願いいたします。
抗悪性腫瘍薬開発フォーラム
代表
武藤徹一郎
公益財団法人がん研究会
第19回抗悪性腫瘍薬開発フォーラムについて
昨年12月に制定された「人を対象とする医学系研究に関する倫理指針」が、これまでの臨床研究や疫学研究に関する倫理指針に換わって本年4月より施行されました。臨床研究の信頼性の確保等のための法規制なども検討されています。また、今年度より、医療法の改正で制度化された「臨床研究中核病院」の指定や、「人道的見地からの治験への参加」(いわゆる日本版コンパッショネートユース)、「患者申出療養(仮称)」といった新たな保険外併用の仕組みの創設がなされようとしています。
このような臨床研究を取巻く環境の大きな変化に応じて、抗悪性腫瘍薬の臨床開発はどのように展開されるべきなのか、また、開発のための臨床試験に対する支援のあり方について、産学官から最前線で活躍する演者をお招きして、制度等の現状や今後の取組みなどについて講演いただくとともに、新局面を踏まえた、よりよい開発戦略の方向性について考えていきたいと思います。
第19回抗悪性腫瘍薬開発フォーラム
実行委員長 山田 雅信
独立行政法人医薬品医療機器総合機構
開催概要
| 名称 | 第19回抗悪性腫瘍薬開発フォーラム 『臨床研究を取り巻く新局面と臨床試験に対する支援のあり方』 |
|---|---|
| 日時 | 2015年6月20日(土)午後1時~6時15分 |
| 会場 | 吉田富三記念講堂、セミナー室AB (公益財団法人がん研究会がん研究所1F)アクセス 〒135-8550 東京都江東区有明3-8-31 |
| 参加費 | 4,000円(ミキサー費含む) 本フォーラムへの参加は事前登録制となっております。 |
| 参加受付 | 参加受付締切:2015年6月2日(火) ※定員になり次第、締め切らせていただきます。 |
| 参加申込み 方法 |
1. HPより参加登録をする。 2. 事務局より締切後、一週間程度で参加確認書をメールにて送信 3. 当日参加確認書を持参の上、参加費を受付で納入 ※上記の方法がとれない方は事務局にご相談下さい。 |
| 事務局 | 〒135-8550 東京都江東区有明3-8-31 (公財)がん研究会がん化学療法センター 担当:三原 TEL:03-3570-0661 FAX:03-3570-0484 E-mail: atdd-frm@jfcr.or.jp |
第19回抗悪性腫瘍薬開発フォーラム参加登録フォーム
登録を締め切りました。プログラム
第19回フォーラムアンケートまとめ
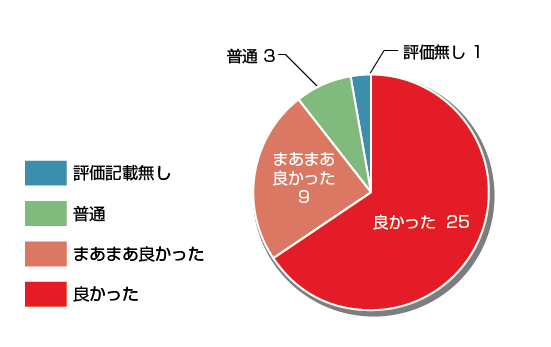
感想・意見
総合評価「良かった&まあまあ良かった」と回答
- CUの問題点、利点が様々な角度から論じられ、分かりやすかった/整理された。(他10件)
- 苦労された方の本音が聞けた→課題がよくわかった。(他3件)
- 共通テーマについて、多角的な意見や情報(検討レベルのものも含め)が聞けたこと。特に官学民の異なる立場から。(他5件)
- 最近の臨床研究を取り巻く制度を全般的に理解でき、問題もわかった。(他3件)
- 森審査管理課長の患者さん中心としつつ、産、学に対して道理をしっかり示す姿勢に対し共感を覚えました。
- 伊藤先生のお話がためになりました。今後、労務提供の行動指針が策定された暁には再度お話を伺いたいです。(CUについての最新情報と合わせて)
- 製薬企業としては人道的見地からの治験参加に関して、より具体的な運用面での指針が官の方からもう少し説明していただきたかったです。
- Q&Aの時間が十分あってよかった。
- 質疑パートは演者を壇上に上げて、パネルディスカッション形式にしてみると盛り上がるのでは。
- 各パートごとに討論すべき。
総合評価「普通&あまり良くなかった」と回答
- 多くの制度を別々に議論されたので、実際のケースにぶつかった時にどういう考察が必要なのかディスカッションを聞きたかった。
今後取り上げるべき、興味のあるテーマ
トランスレーショナルリサーチ、早期探索研究
- AMEDによる早期探索研究(基礎→TR→臨床)推進strategy –産官学連携のあり方、Globalをどう動かすか?
- 日本におけるトランスレーショナルリサーチから臨床研究につながった事例など
- トランスレーショナルリサーチの体制整備資金源について
- Pre-clinical dataの必要性はどこまで
希少がん、希少フラクション
- 希少がんの開発推進についての取り組み
- Gene screening system—bankingの作用機序別活用の展望(Cancer Cell signaling、Stem cell、Immune therapy、Vascularity)
- CoDXのup to date
免疫療法
- 免疫療法の開発戦略(評価方法について)
- 免疫療法の今後の運用について、ガイドライン、コンセンサス、副作用マネジメント
治験、臨床試験
- 治験のQA/QCとは?
- 早期承認プログラムで治験はどう変わるか?
- 企業治験計画時の施設選定の際のマッチングの精度をあげる方策を考えたいです。昨今医療機関側のリソース不足で、治験が進まないことが多くあります。特にオンコロジー領域ではKOLのところに治験が集まりやすくそのような施設では、慢性的なリソース不足が起こっています。治験や臨床試験のリソースがあり、施設としてモチベーションが高い施設を認定とまでは至らずとも、公表するような仕組みがあれば、医療機関と治験とのミスマッチがなくなり、開発がより加速すると思います。「中核病院」に認定されための基準がかなり厳しいようですので、それ以外の方法でも(特に論文数が多くなくても)、治験を依頼するための判断材料となる公表の方法が整備されるとありがたいです。
- 先端医療B で認められず、IIRよりIICTを求められるケースが増えているようです。IICTの治験薬費用提供のベスプラを紹介いただけると助かります。
- 国際競争力にフォーカスした「企業の組織作り、共通プラットフォームの企業間協力」をテーマに各Functionの発表(研究部門、前臨床、早期開発、臨床開発、臨床薬理、Project management、DM統計解析部)
CU、臨床研究を取り巻く環境について
- 今日のようなテーマの続き
- 今日のテーマのようにその時々での「新局面」(今日で言えばCU制度等、支援)について情報交換できるテーマであって欲しい
- CUは継続的にお願いします。
- 混合診療はどう医療を変えるか?
- 研究者主導臨床グループ、学会のあり方
- 専門医制度と臨床試験
規制、承認、制度ほか
- 抗悪ガイドライン
- 承認について
- 制度のup to date
- 医療制度について(テーラーメードや薬価の観点を含めて)
- 医療経済評価の位置付け
- Financial toxcitiesをどう考えるべきか?
- 事例研究
- 常にup to date なものをお願いいたします。
第19回フォーラム実行委員会
| 委員長 | 山田 雅信 ((独)医薬品医療機器総合機構) |
| 副委員長 | 土井 俊彦 (国立がん研究センター東病院) 大熊 伸一 (米国研究製薬工業協会/日本イーライリリー株式会社) |
| 委員 | 春日 芳朋 (欧州製薬団体連合会/中外製薬株式会社) 北川 洋 (欧州製薬団体連合会/ノバルティスファーマ株式会社) 河野 典厚 (厚生労働省) 柴辻 正喜 ((独)医薬品医療機器総合機構) 白鳥 真一 (米国研究製薬工業協会/MSD株式会社) 高橋 俊二 ((公財)がん研究会) 橋本 順一 (日本製薬工業協会/大塚製薬株式会社) 藤田 育子 (欧州製薬団体連合会/バイエル薬品株式会社) 前田 英紀 (日本製薬工業協会/アステラス製薬株式会社) 清宮 啓之 ((公財)がん研究会) 冨田 章弘 ((公財)がん研究会) 藤田 直也 ((公財)がん研究会) |