ごあいさつ
第11回の抗悪性腫瘍薬開発フォーラムを、2011年6月18日(土)に開催致します。
今回のフォーラムは実行委員長に大橋靖雄先生(東京大学)、副委員長に川口政良様(日本製薬工業協会)をお迎えして、「抗悪性腫瘍薬開発における最新の方法論~日本からエビデンスを発信するために~」をテーマに、アダプティブ・デザインをキーワードに、フレキシブルな治験・臨床試験について議論するべく準備を進めております。
是非ご参加いただけますようお願い致します。
抗悪性腫瘍薬開発フォーラム
代表 武藤徹一郎
公益財団法人がん研究会
開催概要
| 名称 | 第11回抗悪性腫瘍薬開発フォーラム 「抗悪性腫瘍薬開発における最新の方法論~日本からエビデンスを発信するために~」 |
|---|---|
| 日時 | 2011年6月18日(土)午後1時~6時 |
| 会場 | 吉田富三記念講堂(公益財団法人がん研究会がん研究所1F)アクセス 〒135-8550 東京都江東区有明3-8-31 |
| 参加費 | 3,000円(ミキサー費含む) 本フォーラムへの参加は事前登録制となっております。 |
| 参加受付しめ切り | 2011年5月27日(金) |
| 参加申込み 方法 |
1. HPより参加登録をする。 2. 事務局より締切一週間程度で参加確認書をメールにて送信 3. 当日参加確認書を持参の上、参加費を受付で納入 *上記の方法がとれない方は事務局にご相談下さい。 |
| 事務局 | 〒135-8550 東京都江東区有明3-8-31 (公財)がん研究会・がん化学療法センター 担当:三原 TEL:03-3520-0111(内線:5415) FAX:03-3570-0484 E-mail: atdd-frm@jfcr.or.jp |
第11回抗悪性腫瘍薬開発フォーラム参加登録フォーム
参加は締め切りました。プログラム
第11回フォーラムアンケートまとめ
第11回抗悪性腫瘍薬開発フォーラムにご参加いただき、またアンケートに対し大変多くの貴重なご意見をいただきまして、誠にありがとうございました。
これらの貴重なご意見は、フォーラム運営サイドのみではなく、参加いただきました諸先生方とシェアすることにより、今後のフォーラムの発展により役に立つものと考えております。なお、本アンケート結果のまとめは、同様なご意見をひとつにまとめるなど、必ずしも原文と同一ではないこと、ご了承ください。
今後ともフォーラムへのご支援賜りますよう、どうぞよろしくお願い申し上げます。
第11回抗悪性腫瘍薬開発フォーラム 実行委員会
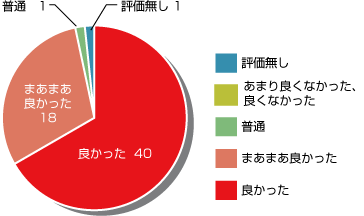
今回のフォーラムの総合評価について
 回答数:60
回答数:60
良かった:40
まあまあ良かった:18
普通:1
あまり良くなかった、良くなかった:0
評価無し:1
感想・意見
- 総合評価「良かった&まあまあ良かった」と回答
- 座長の大橋先生のコメントが適切で、とても内容を理解するのに役立った。(他3件)
- 新しいstudyの取り組み、方向性について産官学の立場からの意見を知ることができた。(他11件)
- 医療経済、治験の合理性/コスト/効率性に焦点が当たった。統計を軸にした機会は初めてで有意義だった。(他9件)
- ベイズ統計、アダプティブデザインの説明が大変わかりやすく良かった。(他14件)
- 原理と実例という構成がわかりやすくて良かった、発表時間もちょうど良かった。(他10件)
- もう少し具体事例を詳細に聞きたかった。(他1件)
今後取り上げるべき、興味のあるテーマ
| バイオマーカーについて |
|
|---|---|
| 国際共同治験、アジアでの開発について |
|
| 治験・臨床試験について |
|
| 規制について |
|
| その他 |
|
第11回フォーラム実行委員会
| 委員長 | 大橋 靖雄 | 東京大学 |
|---|---|---|
| 副委員長 | 川口 政良 | 日本製薬工業協会/エーザイ株式会社 |
| 委員 | 植村 昭夫 | 米国研究製薬工業協会/日本イーライリリー株式会社 |
| 小野田美代子 | 欧州製薬団体連合会/グラクソ・スミスクライン株式会社 | |
| 春日 芳朋 | 欧州製薬団体連合会/中外製薬株式会社 | |
| 粕谷美南子 | 米国研究製薬工業協会/ファイザー株式会社 | |
| 鈴木 正紀 | 日本製薬工業協会/第一三共株式会社 | |
| 澤田 高志 | 日本製薬工業協会/エーザイ株式会社 | |
| 島田 安博 | 国立がん研究センター中央病院 | |
| 朝戸 臣敬 | 欧州製薬団体連合会/サノフィ・アベンティス株式会社 | |
| 橋本 順一 | 日本製薬工業協会/ファイザー株式会社 | |
| 松浦 義昌 | COTEC/中外製薬株式会社 | |
| 森 和彦 | (独)医薬品医療機器総合機構 | |
| 冨田 章弘 | (財)がん研究会 | |
| 清宮 啓之 | (財)がん研究会 | |
| 藤田 直也 | (財)がん研究会 |