
第39回フォーラムアンケートまとめ
【総合評価】
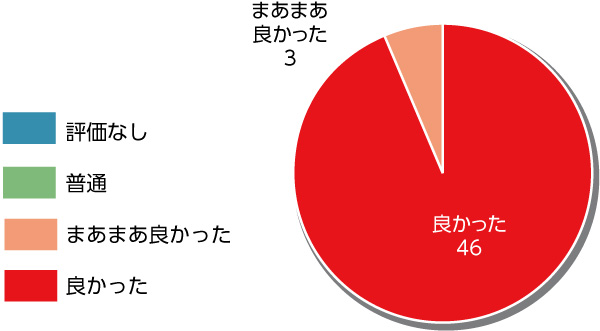
【感想・意見】
「良かった」と回答
- 担当業務を実施する上で勉強になった
- 産官学連携で日本の医療が変わる可能性を感じたため
- CDx、CGPの考えがまとめられた
- CDx開発の課題が整理できました。
- 産官学それぞれの立場からの問題の経緯や今後の課題が見えてきて大変参考になりました。
- CDxおよびCGPについて,現状出来ることと問題点,そして将来の展望について,医療現場・当局・製薬企業の各視点から発表いただけたことで,非常に理解が深まりました。
- それぞれの立場からのコメントが聞けた点。2〜3部では是非診断薬会社の立場からも話を聞きたかったが、やはり立場としてコメントが難しいのは理解できる。
- CDx,CGPだけでなく,LDTも含めて包括的に診断薬の議論が,各ステークホルダー間でできたため。
- LDTというポイントについて今後、治験の中や新薬承認の中での当該性能成績の取り扱い、その後の保険償還についてどういう枠組みで本邦においてフレームが設計されるのか検討するポイントが見えてきた点はプラス評価となりました。
- 第1部に関しては、最先端の情報を得ることができました。第2部以降は身近な話題でしたが、とても濃厚な情報と活発な議論でとても勉強になりました。会場の企業の方が活発にご質問されていて、聞きたかった内容をご質問してくださったので、大変助かりました。第三部のパネルディスカッションにおいても、様々な課題の中でどのように整理して、今後につなげていくとよいか、どのように各先生方がお考えか聞ける大変良い機会となりました。各演者の先生方及びフォーラム実行委員会の先生方に感謝いたします。
- まさに、希少がんのコンパニオン診断薬について問題に直面しているところでしたので、非常に勉強になりました。ありがとうございました。
- 検査環境への医薬品開発者の関心がここまで高いことを知った。様々な課題と動きがあることを知ることができ勉強になりました。
- 診断と治療の関連性の構築をどのように進めていくか、現状を知る良い機会となった。
- 数年先の未来が見られた気がします。
「まあまあ良かった」と回答
- コンパニオン診断薬についての今後の展望が聞けたので。
- Web参加からのQ&Aを取り上げて欲しかった。QA時の木村先生の発言がマイクのスイッチが入っておらず聞こえなかったため、その部分をもう一度回答させて欲しかった。現地を重視し過ぎているようにみえたので双方向でお願いします。
【今後取り上げるべき、興味のあるテーマ】
【コンパニオン診断(CDx)ほか】
- CDx、LDTについて引き続き議論していきたいです。
- ある程度の期間をおいてから、今回のCDxとCGPの問題の続きをお願いできれば幸いです。
- 特に体外診断薬において、審査〜承認〜保険適用までの期間が、標準で18か月(審査12か月+保険適用6か月)かかることで、医薬品の標準期間とずれが起こっており、同時の上市が難しい現状があることについての課題について議論いただきたいです。
- CDxに対する様々な問題点があることが分かりましたが、規制上あまり柔軟性がないように感じました。今後の動きについても引き続き取り上げていただければ幸いです。
- LDTを臨床実装するために,何を決定するべきか,誰が何をいつするべきか,各ステークホルダー(保険の部分も含め)間で議論をし,早期臨床実装へつなげる。
- 全ゲノムの可能性
【抗がん剤開発の現状と今後】
- 本法における抗がん剤開発の現状と今後の展望を改めて議論していただきたい
- 希少疾患の開発
- 小児がん開発の現在地
- Theranostics
【アジアの中の抗悪性腫瘍薬の開発について】
- 中国発データの取り扱い(同じアジア人としての評価、その活用):中国発医薬品の導入の場合、どこまで日本人での追加評価が必要かの整理/日本で症例集積が難しい、またはデータがない場合のアジア人データの活用
- 5年後も海外(中国等)と比較して競争力を維持するためにできること
【規制・制度】
- 薬機法で規定された条件付き承認制度の希少がん領域での評価と承認審査での取り扱いについて
- 今回も先端的な事例を取り上げてくださりとても勉強になりました。規制当局のコメントが、従前に比べとても柔軟性を感じさせるもので、一緒に開発を進めたいとの意欲を感じさせてくれました。
【医療経済・医療技術評価】
- HTA評価、薬価について
- 薬価制度、現状の医療費や海外の薬価、医療費制度を踏まえた新薬開発の課題を勉強したく思いました
【その他】
- 腫瘍診断は国際的に均てん化されているのか?
- がん検診
Page Top


